什麼是Nrf2?
國家衛生研究院
郭博士長期以來並投注大量心力於探討NF-E2相關因子2(nuclear factor erythroid-2-related factor, Nrf2)在腫瘤的化學預防、癌化進展,以及抗藥衍生所扮演之角色;並藉由這些研究,進一步開發出具有潛力的化學預防以及逆轉抗藥性之新穎治療策略。Nrf2為一種對氧化還原反應敏感之轉錄因子,活化的Nrf2透過與氧化反應元件(antioxidant response element, ARE)相互作用,可活化許多代謝解毒酵素與抗氧化蛋白,在抑制癌化與抗氧化等細胞防禦保護中發揮重要的作用。口腔癌為台灣本土性的醫療問題,抽菸、喝酒、嚼檳榔誘發自由基且協同石灰誘導的細胞增生作用,目前被認為是口腔鱗狀細胞癌化的機制之一,因此,開發新穎的Nrf2活化劑,活化人體抗氧化之防禦機制,可作為口腔癌化學預防的重要策略;此策略也是藥廠看重的方向,如亞培(Abbott)投注大量資金進行Nrf2活化劑的研發。因此,郭博士看重此潛力與契機,於癌症研究所主導這項研究。首先,在模式的建立以及第一代Nrf2活化劑的篩選工作中,郭博士自許多具新穎化學骨架的抗氧化劑以及抗致突變劑,開發出新穎的Nrf2活化劑,並闡明部分具有潛力的Nrf2活化劑,其上游訊息路徑的調節、抗氧化防禦機制與重要下游調控的分子標的,以及證明部分Nrf2活化劑確實能有效地阻斷口腔癌化因子(包括菸、酒、檳榔)所誘發的傷害。因此,Nrf2活化劑應有潛力成為阻斷口腔癌化的癌症化學預防物質。
儘管Nrf2在正常細胞的活化能阻斷致癌劑所誘導的傷害,但活化的Nrf2可調節ARE基因產物的表達(包括第二類代謝解毒酵素、抗氧化蛋白、藥物外排蛋白基因等),這樣的結果將導致腫瘤細胞對化學治療的敏感性減低,雖然有許多研究指出Nrf2對抗藥衍生具有重要調控角色,但是細部的調控,以及到底是那一個ARE基因,實際仲介不同抗癌藥物的抗藥衍生卻乏人研究。郭博士的研究團隊首次發現Nrf2可藉由不同下游ARE基因的調控,引發不同抗癌藥物的抗藥衍生機制,包括Nrf2/ABCC1 axis in Topo II poisons、Nrf2/GR axis in paclitaxel,以及Nrf2/AKR1Cs axis in oxaliplatin。其中Nrf2/AKR1Cs in oxaliplatin resistance的研究,於2012年6月在韓國首爾舉行的「10th International Conference of the Asia Clinical Oncology Society」中,榮獲大會頒發「Merit Award」,顯示郭博士對Nrf2的研究有許多重要與新穎的斬獲,深受國際專家學者之肯定。未來郭博士將更深入的闡明Nrf2在化療衍生的面相與細微的調節,並根據這些結果作為開發有用治療策略之利基。
儘管Nrf2在正常細胞的活化能阻斷致癌劑所誘導的傷害,但活化的Nrf2可調節ARE基因產物的表達(包括第二類代謝解毒酵素、抗氧化蛋白、藥物外排蛋白基因等),這樣的結果將導致腫瘤細胞對化學治療的敏感性減低,雖然有許多研究指出Nrf2對抗藥衍生具有重要調控角色,但是細部的調控,以及到底是那一個ARE基因,實際仲介不同抗癌藥物的抗藥衍生卻乏人研究。郭博士的研究團隊首次發現Nrf2可藉由不同下游ARE基因的調控,引發不同抗癌藥物的抗藥衍生機制,包括Nrf2/ABCC1 axis in Topo II poisons、Nrf2/GR axis in paclitaxel,以及Nrf2/AKR1Cs axis in oxaliplatin。其中Nrf2/AKR1Cs in oxaliplatin resistance的研究,於2012年6月在韓國首爾舉行的「10th International Conference of the Asia Clinical Oncology Society」中,榮獲大會頒發「Merit Award」,顯示郭博士對Nrf2的研究有許多重要與新穎的斬獲,深受國際專家學者之肯定。未來郭博士將更深入的闡明Nrf2在化療衍生的面相與細微的調節,並根據這些結果作為開發有用治療策略之利基。
Nrf2抗氧化抗炎系統和腫瘤預防
抗氧化劑包括直接中和自由基和抑制活性氧產生兩類。在生物系統,活性氧和抗氧化系統是一種動態平衡,抗氧化系統包括酶和非酶抗氧化劑。抗氧化劑直接中和自由基維持細胞內氧化還原狀態,非酶抗氧化物質包括維生素C、維生素E、維生素A、硒、多酚,以及羥基抗氧化劑如谷胱甘肽、硫氧化還原蛋白和硫辛酸。維生素C是水溶性抗氧化劑和輔酶因子,存在與許多植物和一些動物體內。人類自身不能合成維生素C,必須通過飲食攝取維持平衡(老虎獅子自己能合成,不需要補充)。維生素C有兩種化學形式,氧化型(脫氫)和還原型抗壞血酸。還原型維生素C是人體內主要的存在形式,具有抗氧化作用,能有效清除自由基。許多在體研究發現,維生素C具有預防和治療癌症的作用。但是,高濃度維生素C可作為促氧化劑增加活性氧的產生。維生素C和維生素E聯合能維護細胞膜內生育酚自由基的再生。維生素E是脂溶性抗氧化劑,有8種不同存在形式,維生素E不僅有抗氧化作用,也具有促氧化作用。
抗氧化酶包括SOD、過氧化氫酶和谷胱甘肽過氧化物酶(GPxs)。SOD是抗氧化系統的重要成員,有三種形式分別是細胞漿Cu/ZnSOD、線粒體MnSOD 和細胞外Cu/ZnSOD。所有SOD都需要金屬離子作為活性中心。過氧化氫酶可將過氧化氫降解為水和氧氣。谷胱甘肽硫轉酶(GSTs)和GPxs是在抗氧化損傷中具有重要作用。巰基小分子包括谷胱甘肽(GSH)是細胞內重要的抗氧化劑,γ谷氨酸半胱氨酸合成酶(γGCS)包括谷氨酸半胱氨酸連接酶(Gcl)、催化和修飾亞單位,是合成GSH的限速酶。一些巰基小分子如Txn和谷氧還蛋白可作為抗氧化酶的底物發揮抗氧化作用。另外,谷胱甘肽還原酶和NADPH醌氧化還原酶1、UDP葡糖醛酸基轉移酶和硫氧還蛋白還原酶也都屬於抗氧化酶,在巰基的循環利用中發揮作用。
在抗氧化系統中,一些壓力反應蛋白如血紅素加氧酶、金屬硫蛋白和熱休克蛋白可以提供對抗各種氧化損傷。
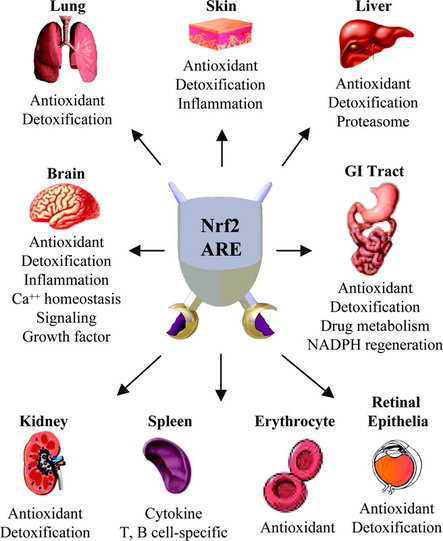
大部分抗氧化基因都包括抗氧化反應元件(ARE),ARE的共同序列為5′-RTGAYnnnGCR-3(其中R = A or G, Y = C or T)。轉錄因子Nrf2可以和ARE結合,促進抗氧化基因的轉錄。Nrf2是1994年首次在血紅素誘導的紅系K562細胞中被鑑定出來的,Nrf2屬於亮氨酸拉鏈核轉錄因子家族,和果蠅CNC(Cap n' Collar)家族同源,人類Nrf2和核因子紅系2亞單位p45高度同源。Nrf2基因敲除小鼠解毒酶水平降低,對環境毒素和異生物質損傷更敏感。Nrf2活性主要受Keap1調節,Keap1和果蠅actin結合蛋白Kelch同源。正常情況下,Nrf2被Keap1限制在細胞漿內。當細胞受到氧化或化學壓力時,Nrf2和Keap1分離並轉入細胞核,在細胞核內和其他同源亮氨酸拉鏈蛋白,如Maf、激活轉錄因子(ATF)或AP-1家族亮氨酸拉鏈蛋白等,結合為異源二聚體,啟動目標基因的轉錄。
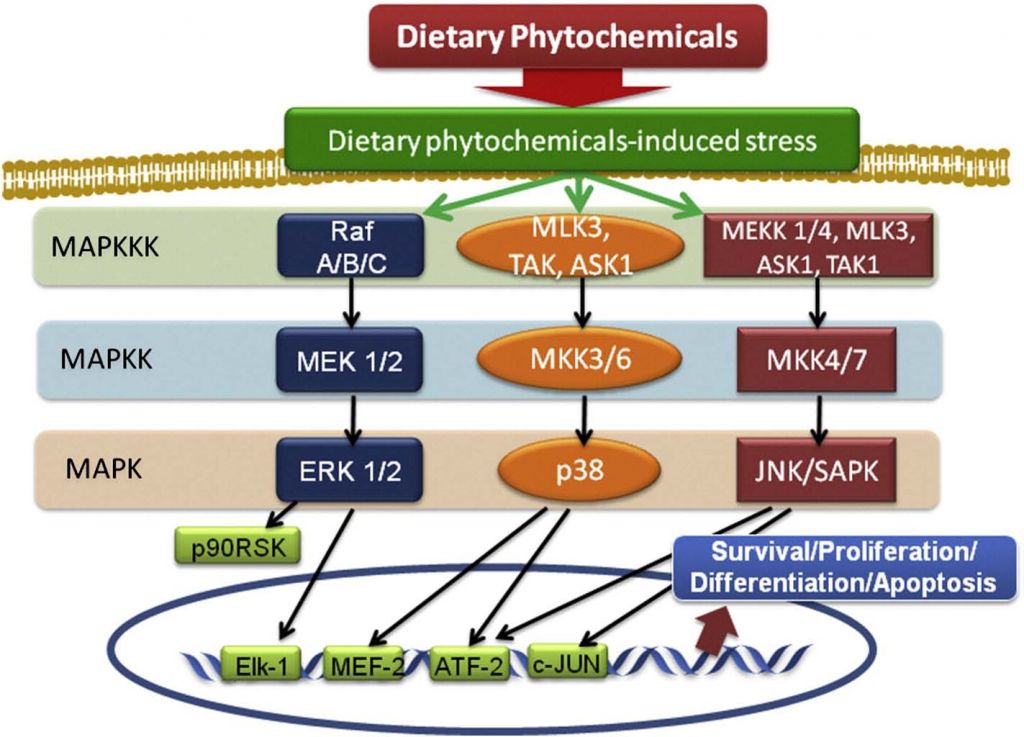
許多細胞信號通路參與Nrf2系統的調節,MAPK通路中各種分子包括ERK、JNK和p38,以及PKC和PI3K都參與Nrf2–Keap1激活。研究發現,ERK 和JNK能促進ARE介導的效應,Nrf2被p38磷酸化則可加強Keap1/Nrf2結合,抑制Nrf2活性。PKC可以直接磷酸化Nrf240位絲氨酸,PI3K可促進Nrf2核轉位。MAPK雖然也可直接磷酸化Nrf2,但對Nrf2的核轉位和活性影響較小。氧化壓力是Nrf2活性調節的重要促進因素。
抗氧化酶包括SOD、過氧化氫酶和谷胱甘肽過氧化物酶(GPxs)。SOD是抗氧化系統的重要成員,有三種形式分別是細胞漿Cu/ZnSOD、線粒體MnSOD 和細胞外Cu/ZnSOD。所有SOD都需要金屬離子作為活性中心。過氧化氫酶可將過氧化氫降解為水和氧氣。谷胱甘肽硫轉酶(GSTs)和GPxs是在抗氧化損傷中具有重要作用。巰基小分子包括谷胱甘肽(GSH)是細胞內重要的抗氧化劑,γ谷氨酸半胱氨酸合成酶(γGCS)包括谷氨酸半胱氨酸連接酶(Gcl)、催化和修飾亞單位,是合成GSH的限速酶。一些巰基小分子如Txn和谷氧還蛋白可作為抗氧化酶的底物發揮抗氧化作用。另外,谷胱甘肽還原酶和NADPH醌氧化還原酶1、UDP葡糖醛酸基轉移酶和硫氧還蛋白還原酶也都屬於抗氧化酶,在巰基的循環利用中發揮作用。
在抗氧化系統中,一些壓力反應蛋白如血紅素加氧酶、金屬硫蛋白和熱休克蛋白可以提供對抗各種氧化損傷。
大部分抗氧化基因都包括抗氧化反應元件(ARE),ARE的共同序列為5′-RTGAYnnnGCR-3(其中R = A or G, Y = C or T)。轉錄因子Nrf2可以和ARE結合,促進抗氧化基因的轉錄。Nrf2是1994年首次在血紅素誘導的紅系K562細胞中被鑑定出來的,Nrf2屬於亮氨酸拉鏈核轉錄因子家族,和果蠅CNC(Cap n' Collar)家族同源,人類Nrf2和核因子紅系2亞單位p45高度同源。Nrf2基因敲除小鼠解毒酶水平降低,對環境毒素和異生物質損傷更敏感。Nrf2活性主要受Keap1調節,Keap1和果蠅actin結合蛋白Kelch同源。正常情況下,Nrf2被Keap1限制在細胞漿內。當細胞受到氧化或化學壓力時,Nrf2和Keap1分離並轉入細胞核,在細胞核內和其他同源亮氨酸拉鏈蛋白,如Maf、激活轉錄因子(ATF)或AP-1家族亮氨酸拉鏈蛋白等,結合為異源二聚體,啟動目標基因的轉錄。
許多細胞信號通路參與Nrf2系統的調節,MAPK通路中各種分子包括ERK、JNK和p38,以及PKC和PI3K都參與Nrf2–Keap1激活。研究發現,ERK 和JNK能促進ARE介導的效應,Nrf2被p38磷酸化則可加強Keap1/Nrf2結合,抑制Nrf2活性。PKC可以直接磷酸化Nrf240位絲氨酸,PI3K可促進Nrf2核轉位。MAPK雖然也可直接磷酸化Nrf2,但對Nrf2的核轉位和活性影響較小。氧化壓力是Nrf2活性調節的重要促進因素。
飲食和草藥中的植物活性物在預防癌症中的作用逐漸受到重視。這些物質在癌症預防和輔助化療中的作用可以從細胞學研究中獲得證據。許多黃酮和多酚抗氧化物,如兒茶素和薑黃素表現出抗氧化和抗炎症效應,這些效應是通過Nrf2相關的二相解毒酶和抗氧化酶產生。同一種物質往往表現出多種效應,如薑黃素不僅能通過阻斷I B降解抑制NF B發揮抗炎效應,通過抑制Akt和ERK磷酸化促進抗氧化反應,也可通過抑制TNF和Bcl-2表達影響細胞死亡。
氧化壓力是活性氧產生和細胞抗氧化能力失衡的表現,氧化壓力可造成蛋白、核酸和脂類分子損傷,導致多種病理效應,如炎症和癌症。細胞內抗氧化系統能緩衝活性氧的毒性。巰基小分子如GSH和 Txn屬於非酶抗氧化系統,能直接中和活性氧。酶抗氧化系統如過氧化氫酶、GPx、過氧化物酶能催化GSH和 Txn和活性氧反應。來自藥物異生物質、致癌物和環境毒素可通過一相酶如細胞色素P450產生有毒的親核或親電子疏水代謝產物。這些代謝產物大多數會在二相解毒或抗氧化酶協助下和親水分子如GSH和葡萄糖醛酸結合併被降解。
Nrf2是二相解毒或抗氧化酶核心調節因子,能保護細胞避免發生氧化損傷。因此,植物活性物能通過二相解毒或抗氧化酶表達提高細胞抗氧化能力。
1 Nrf2抗氧化解毒系統
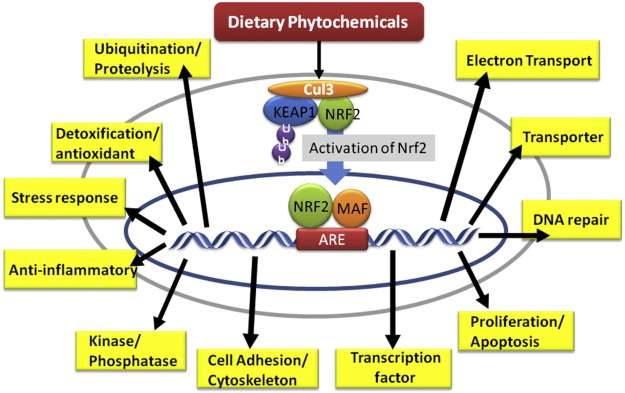
Nrf2抗氧化解毒系統,或二相抗氧化解毒酶主要包括結合酶如GST和UGT、還原酶NQO和壓力反應酶如HO-1。大部分二相抗氧化解毒酶通過ARE調節,Nrf2是結合ARE的基本轉錄因子。Nrf2從細胞漿轉位到細胞核和其他同源轉錄因子結合,共同激活ARE。許多化學物質能通過Nrf2誘導ARE的目標基因表達,這些物質包括BHA、叔丁基羥基醌、異硫氰酸鹽蘿蔔硫素和三萜類齊墩果烷等。
有7種不同類型的GST是內源性和外源性親電子體的清除劑,這些親電子體包括環氧化合物、醛類和過氧化物。Nrf2是GST的關鍵調節因素,能誘導多種類型的GST基因表達,Nrf2基因敲除動物GST蛋白和mRNA均明顯下調,Keap1基因敲除動物肝臟Nrf2活性和GST mRNA表達水平上調。BHA和乙氧喹可誘導Nrf2提高小鼠肝臟GST mRNA表達,一種強毒性膽汁酸石膽酸也能產生同樣的效應。
UGT可結合外源性(藥物、農藥和致癌物)和內源性有毒物質(膽紅素和激素等),並轉化為水溶性葡糖苷酸物質進行排泄。UGT是機體對抗環境有毒化學物質和致癌物的關鍵系統。UGT缺乏皮膚成纖維細胞對致癌物苯並芘的敏感性提高。乳腺癌細胞內DMBA–DNA交聯物和UGT1A1增加。tBHQ能誘導小鼠肝臟和小腸內UGT1A1基因表達水平。Nrf2基因敲除動物多種UGT基因表達和酶活性水平下調。Nrf2可上調UGT活性提高吸菸動物肝臟內4聯苯胺和葡萄糖醛酸結合,保護4聯苯胺引起的肝損傷。奧替普拉能提高這些酶基因表達和活性,但不能影響Nrf2基因敲除動物該基因表達。
NQO1是一種細胞漿黃素蛋白,能利用醌類還原解毒內源性和外源性毒物。NQO1破壞會增加細胞對致癌物敏感性,Nrf2基因敲除動物該基因表達和酶活性均下調。
環磷酰胺的早期致癌作用能引起大鼠肝臟氧化壓力,蝦青素可通過Nrf2誘導NQO-1和HO-1的表達對抗這種氧化損傷。番茄紅素代謝物也可誘導人類肝癌HepG2細胞Nrf2核轉位,促進NQO-1和HO-1的表達。薑黃素可通過Nrf2啟動子序列CpG島去甲基化,促進Nrf2基因表達,提高NQO1基因和蛋白表達水平。
HO-1具有抗氧化和抗炎症效應,能催化亞鐵血紅素代謝成為一氧化碳和膽紅素,一氧化碳和膽紅素具有抗氧化和抗炎作用。氧化壓力可通過Nrf2途徑誘導HO-1基因和蛋白表達水平,百草枯和氯化鎘能誘導小鼠外周巨噬細胞HO-1基因和蛋白表達,Nrf2基因敲除動物則無法產生這種作用。去甲二氫愈創木酸(NDGA)是一種腫瘤預防劑,可誘導多種細胞表達Nrf2 和 HO-1。黃連素也能通過Nrf2促進HO-1基因和蛋白表達。
2 Nrf2的抗炎效應
因為炎症反應和氧化壓力幾乎就是孿生兄弟。所以Nrf2不僅是抗氧化系統的總司令,在抗炎症方面也發揮關鍵作用。
LPS可以提高NADPH氧化酶依賴的活性氧生成,提高TNF、IL-6 和Mcp-1等關鍵炎症因子表達,在Nrf2基因敲除動物,這種效應明顯增強。Nrf2是固有免疫反應的關鍵調節因子,Nrf2基因敲除動物膿毒症死亡率明顯增加。Nrf2系統和炎症反應存在密切聯繫,炎症信號能負向調節Nrf2系統。有人提出,NFκB能通過選擇性阻斷Nrf2和CREB的結合,NFκB也能通過促進HDAC3與CBP或MafK的作用,抑制Nrf2/ARE活性。
Nrf2能緩解化學誘導性肺損傷和炎症反應。Nrf2基因敲除動物更容易受到菸草誘導發生呼吸道炎症、肺氣腫和哮喘,促進支氣管和脾臟內Th2細胞因子IL-4和IL-13的表達和肺泡上皮細胞凋亡,這些表現的關鍵原因是由於抗氧化基因表達水平下降。Nrf2基因敲除小鼠對DSS誘導的結腸炎更敏感,發病率、結腸隱窩丟失、炎症細胞浸潤、便血等表現都明顯增加。Nrf2基因敲除小鼠各種抗氧化酶活性降低,但炎症相關因子如(IL)-1β、IL-6, TNF-α、iNOS和 COX2都顯著增加。激活Nrf2系統能預防動物炎症損傷,這也正是這類物質預防癌症的根本原因。
氧化壓力是活性氧產生和細胞抗氧化能力失衡的表現,氧化壓力可造成蛋白、核酸和脂類分子損傷,導致多種病理效應,如炎症和癌症。細胞內抗氧化系統能緩衝活性氧的毒性。巰基小分子如GSH和 Txn屬於非酶抗氧化系統,能直接中和活性氧。酶抗氧化系統如過氧化氫酶、GPx、過氧化物酶能催化GSH和 Txn和活性氧反應。來自藥物異生物質、致癌物和環境毒素可通過一相酶如細胞色素P450產生有毒的親核或親電子疏水代謝產物。這些代謝產物大多數會在二相解毒或抗氧化酶協助下和親水分子如GSH和葡萄糖醛酸結合併被降解。
Nrf2是二相解毒或抗氧化酶核心調節因子,能保護細胞避免發生氧化損傷。因此,植物活性物能通過二相解毒或抗氧化酶表達提高細胞抗氧化能力。
1 Nrf2抗氧化解毒系統
Nrf2抗氧化解毒系統,或二相抗氧化解毒酶主要包括結合酶如GST和UGT、還原酶NQO和壓力反應酶如HO-1。大部分二相抗氧化解毒酶通過ARE調節,Nrf2是結合ARE的基本轉錄因子。Nrf2從細胞漿轉位到細胞核和其他同源轉錄因子結合,共同激活ARE。許多化學物質能通過Nrf2誘導ARE的目標基因表達,這些物質包括BHA、叔丁基羥基醌、異硫氰酸鹽蘿蔔硫素和三萜類齊墩果烷等。
有7種不同類型的GST是內源性和外源性親電子體的清除劑,這些親電子體包括環氧化合物、醛類和過氧化物。Nrf2是GST的關鍵調節因素,能誘導多種類型的GST基因表達,Nrf2基因敲除動物GST蛋白和mRNA均明顯下調,Keap1基因敲除動物肝臟Nrf2活性和GST mRNA表達水平上調。BHA和乙氧喹可誘導Nrf2提高小鼠肝臟GST mRNA表達,一種強毒性膽汁酸石膽酸也能產生同樣的效應。
UGT可結合外源性(藥物、農藥和致癌物)和內源性有毒物質(膽紅素和激素等),並轉化為水溶性葡糖苷酸物質進行排泄。UGT是機體對抗環境有毒化學物質和致癌物的關鍵系統。UGT缺乏皮膚成纖維細胞對致癌物苯並芘的敏感性提高。乳腺癌細胞內DMBA–DNA交聯物和UGT1A1增加。tBHQ能誘導小鼠肝臟和小腸內UGT1A1基因表達水平。Nrf2基因敲除動物多種UGT基因表達和酶活性水平下調。Nrf2可上調UGT活性提高吸菸動物肝臟內4聯苯胺和葡萄糖醛酸結合,保護4聯苯胺引起的肝損傷。奧替普拉能提高這些酶基因表達和活性,但不能影響Nrf2基因敲除動物該基因表達。
NQO1是一種細胞漿黃素蛋白,能利用醌類還原解毒內源性和外源性毒物。NQO1破壞會增加細胞對致癌物敏感性,Nrf2基因敲除動物該基因表達和酶活性均下調。
環磷酰胺的早期致癌作用能引起大鼠肝臟氧化壓力,蝦青素可通過Nrf2誘導NQO-1和HO-1的表達對抗這種氧化損傷。番茄紅素代謝物也可誘導人類肝癌HepG2細胞Nrf2核轉位,促進NQO-1和HO-1的表達。薑黃素可通過Nrf2啟動子序列CpG島去甲基化,促進Nrf2基因表達,提高NQO1基因和蛋白表達水平。
HO-1具有抗氧化和抗炎症效應,能催化亞鐵血紅素代謝成為一氧化碳和膽紅素,一氧化碳和膽紅素具有抗氧化和抗炎作用。氧化壓力可通過Nrf2途徑誘導HO-1基因和蛋白表達水平,百草枯和氯化鎘能誘導小鼠外周巨噬細胞HO-1基因和蛋白表達,Nrf2基因敲除動物則無法產生這種作用。去甲二氫愈創木酸(NDGA)是一種腫瘤預防劑,可誘導多種細胞表達Nrf2 和 HO-1。黃連素也能通過Nrf2促進HO-1基因和蛋白表達。
2 Nrf2的抗炎效應
因為炎症反應和氧化壓力幾乎就是孿生兄弟。所以Nrf2不僅是抗氧化系統的總司令,在抗炎症方面也發揮關鍵作用。
LPS可以提高NADPH氧化酶依賴的活性氧生成,提高TNF、IL-6 和Mcp-1等關鍵炎症因子表達,在Nrf2基因敲除動物,這種效應明顯增強。Nrf2是固有免疫反應的關鍵調節因子,Nrf2基因敲除動物膿毒症死亡率明顯增加。Nrf2系統和炎症反應存在密切聯繫,炎症信號能負向調節Nrf2系統。有人提出,NFκB能通過選擇性阻斷Nrf2和CREB的結合,NFκB也能通過促進HDAC3與CBP或MafK的作用,抑制Nrf2/ARE活性。
Nrf2能緩解化學誘導性肺損傷和炎症反應。Nrf2基因敲除動物更容易受到菸草誘導發生呼吸道炎症、肺氣腫和哮喘,促進支氣管和脾臟內Th2細胞因子IL-4和IL-13的表達和肺泡上皮細胞凋亡,這些表現的關鍵原因是由於抗氧化基因表達水平下降。Nrf2基因敲除小鼠對DSS誘導的結腸炎更敏感,發病率、結腸隱窩丟失、炎症細胞浸潤、便血等表現都明顯增加。Nrf2基因敲除小鼠各種抗氧化酶活性降低,但炎症相關因子如(IL)-1β、IL-6, TNF-α、iNOS和 COX2都顯著增加。激活Nrf2系統能預防動物炎症損傷,這也正是這類物質預防癌症的根本原因。
3. Nrf2系統和癌症預防
Nrf2控制的二相解毒抗氧化系統激活是各種癌症化學預防方法中最有效的手段。許多膳食抗癌成分都表現出抗氧化及二相解毒抗氧化系統誘導效應。因此Nrf2是最重要的癌症預防目標調節通路。
食物來源的營養成分中,比較確切能活化自體Nrf2系統的物質包括薑黃素、蘿蔔硫素、白黎蘆醇和綠茶提取物等。攝取這些物質能通過提高內源性抗氧化系統和減少炎症反應,提高機體降低各種來自食物藥物和環境來源的致癌物和因素導致的致癌效應。大量動物實驗研究證明這些手段具有潛在的預防效應。
氫氣作為一種選擇性抗氧化物質,但關於抗氧化的具體機制仍不十分清楚,有人也發現這種物質能提高體內抗氧化系統,增加各種抗氧化酶如SOD、CAT、HO-1和GSH活性和水平,也具有激活Nrf2系統的作用。另外氫氣具有明顯的抗炎效應。這些研究說明,氫氣和Nrf2系統存在密切聯繫,許多生物學效應可能是通過Nrf2系統實現的。表面上看,抗氧化物往往對Nrf2系統有直接抑制效應,因為Nrf2系統內源性啟動信號正是氧化壓力本身。但是由於氫雖然能中和有毒自由基的破壞作用,並不影響具有信號作用的活性氧,也就是說氫在對抗氧化損傷的同時,並不干擾氧化壓力信號系統,可在保留氧化壓力啟動內源性抗氧化抗炎症系統的基礎上減少氧化損傷,產生協同效應。這或者就是氫氣神奇效應的基礎。
總結:
自體Nrf2基因的活化能夠修復體內損壞的組織系統以及神經系統,能夠有效達到抗發炎以及癌細胞病變的產生,Nrf2的活化能夠讓人體重新再生產出大量活性梅,例如:穀胱甘肽Glutathione、過氧化氫酶Catalase、超氧化物歧化酶SOD,體內擁有足夠的活性酶能達到抗衰老以及任何疾病的產生,人體的Nrf2基因在20歲就會開始逐漸挺止運作,25歲就終止活性酶的產生,必須透過一些物質來活化Nrf2因子,目前證實透過活化Nrf2因子來達到抗衰老以及疾病的產生是最有效的方法!
Nrf2控制的二相解毒抗氧化系統激活是各種癌症化學預防方法中最有效的手段。許多膳食抗癌成分都表現出抗氧化及二相解毒抗氧化系統誘導效應。因此Nrf2是最重要的癌症預防目標調節通路。
食物來源的營養成分中,比較確切能活化自體Nrf2系統的物質包括薑黃素、蘿蔔硫素、白黎蘆醇和綠茶提取物等。攝取這些物質能通過提高內源性抗氧化系統和減少炎症反應,提高機體降低各種來自食物藥物和環境來源的致癌物和因素導致的致癌效應。大量動物實驗研究證明這些手段具有潛在的預防效應。
氫氣作為一種選擇性抗氧化物質,但關於抗氧化的具體機制仍不十分清楚,有人也發現這種物質能提高體內抗氧化系統,增加各種抗氧化酶如SOD、CAT、HO-1和GSH活性和水平,也具有激活Nrf2系統的作用。另外氫氣具有明顯的抗炎效應。這些研究說明,氫氣和Nrf2系統存在密切聯繫,許多生物學效應可能是通過Nrf2系統實現的。表面上看,抗氧化物往往對Nrf2系統有直接抑制效應,因為Nrf2系統內源性啟動信號正是氧化壓力本身。但是由於氫雖然能中和有毒自由基的破壞作用,並不影響具有信號作用的活性氧,也就是說氫在對抗氧化損傷的同時,並不干擾氧化壓力信號系統,可在保留氧化壓力啟動內源性抗氧化抗炎症系統的基礎上減少氧化損傷,產生協同效應。這或者就是氫氣神奇效應的基礎。
總結:
自體Nrf2基因的活化能夠修復體內損壞的組織系統以及神經系統,能夠有效達到抗發炎以及癌細胞病變的產生,Nrf2的活化能夠讓人體重新再生產出大量活性梅,例如:穀胱甘肽Glutathione、過氧化氫酶Catalase、超氧化物歧化酶SOD,體內擁有足夠的活性酶能達到抗衰老以及任何疾病的產生,人體的Nrf2基因在20歲就會開始逐漸挺止運作,25歲就終止活性酶的產生,必須透過一些物質來活化Nrf2因子,目前證實透過活化Nrf2因子來達到抗衰老以及疾病的產生是最有效的方法!
 RSS Feed
RSS Feed